推荐产品
公司新闻/正文
Nature Neuroscience | NovoCyte助力寻找 IL-17 导致高血压认知障碍的真正“接头人”
450 人阅读发布时间:2024-05-30 13:34
高血压(HTN)是人类主要的慢性病之一,也是认知功能障碍和痴呆症的主要原因之一。我国高血压患者已高达 2.45 亿,其发病机制至今仍不甚明了。美国威尔康奈尔医学院的 Costantino Iadecola 研究团队发现硬脑膜中 T 细胞产生的 IL-17 释放到脑脊液中,并激活边界相关巨噬细胞 BAMs,引发氧化应激并抑制 NO 合成,从而损伤神经血管和认知功能。该研究发表在 Nature Neuroscience。

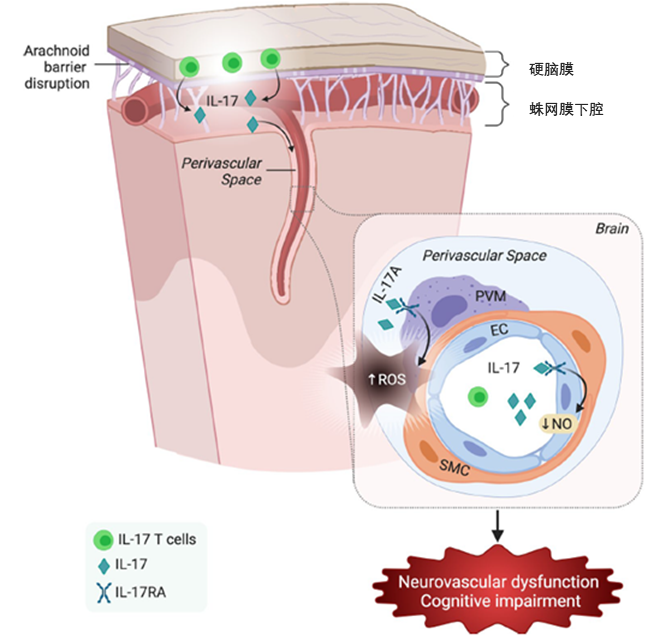
DOCA 盐高血压改变小鼠神经血管和认知功能的机制概述
01 IL-17 介导 DOCA 盐高血压的神经血管和认知功能损伤
研究者应用醋酸脱氧皮质酮盐(DOCA)的高盐饮食诱导盐性高血压小鼠模型进行研究,仅摄入三天小鼠血压明显升高(Fig1a)。随后建立激光多普勒血流测量法测量小鼠大脑血流量(CBF), DOCA 盐高血压小鼠 CBF 在不同刺激以及环境下都明显下降(Fig 1b-f)。同时通过新物体认知和巴恩斯行为学实验发现,DOCA 也会导致小鼠认知能力的损伤(Fig 1g-i)。
基于高血压和高盐饮食循环 IL-17 增多,研究者猜想是否 IL-17 参与 DOCA 盐高血压的神经血管和认知损伤,利用 IL17a locus eGFP 小鼠建立 DOCA 盐高血压模型,多种实验发现摄入 DOCA 后体内 IL-17 明显升高。NovoCyte Quanteon 流式细胞仪对小肠固有层(LP)、淋巴结(LNs)、PBMCs 以及脾脏(SP)的 IL17 分泌 T 细胞:TH17 和 γδT17 细胞进分析,DOCA 摄入后 TH17 和 γδT17 细胞明显增多(Fig 2e-I,Novocyte Quanteon 检测结果)。然而在 IL-17 KO 小鼠中即使摄入 DOCA 也并不影响小鼠 CBF 以及认知功能。
因此,TH17 和 γδT17 细胞产生的 IL-17 对 DOCA 盐高血压的神经血管和认知功能障碍至关重要。
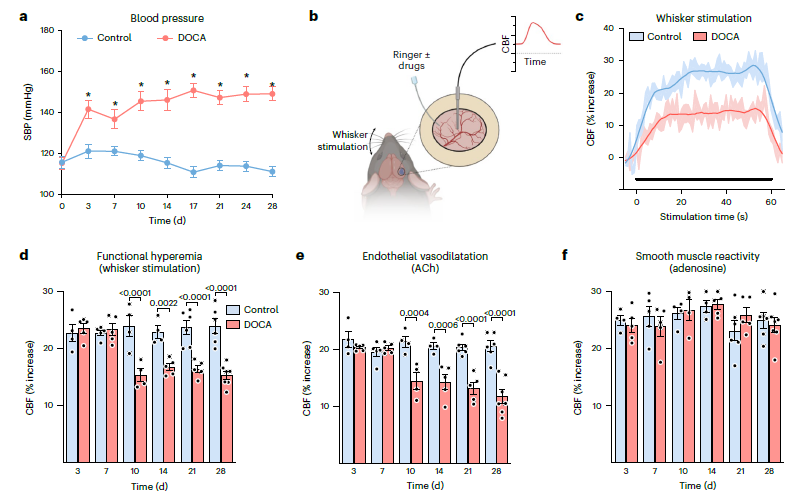
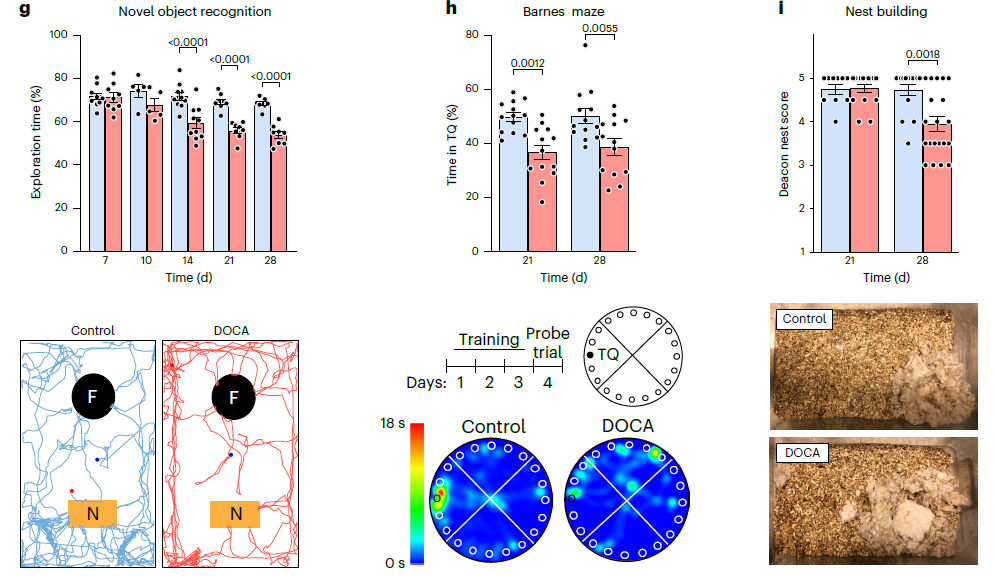
Fig1 . DOCA 盐高血压模型会诱发神经血管和认知障碍
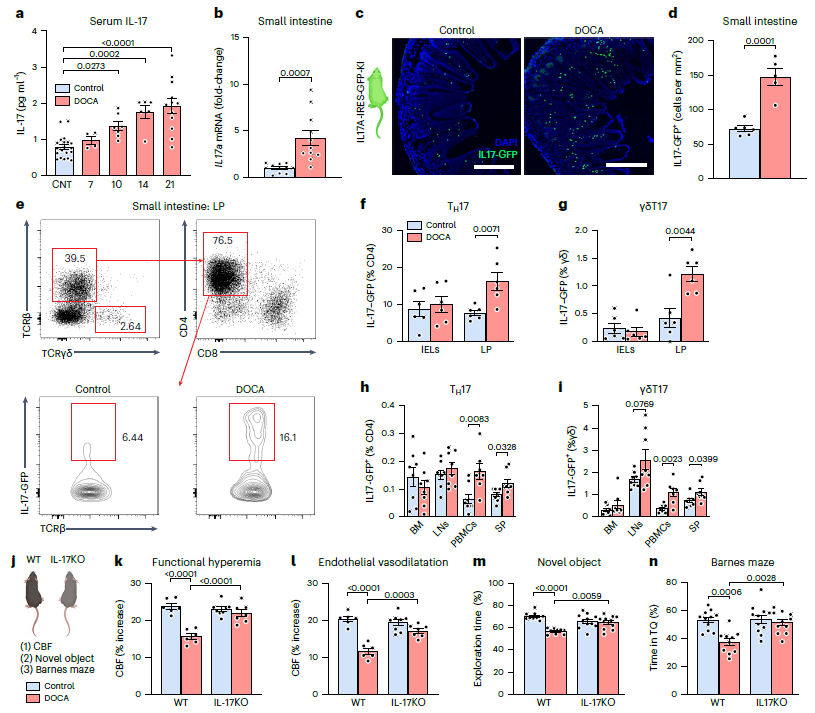
Fig2 . DOCA 诱导的神经血管和认知功能损伤是由 IL-17 介导
02 IL-17RA 产生的 ROS 在 BAMs 中介导了高血压引起大脑功能障碍
研究者敲除脑内皮 IL-17RA 仅部分改善了神经血管和认知功能,而 IL-17 KO 则完全缓解了 DOCA 导致的功能障碍,这表明其他细胞的 IL-17RA 也参与了认知功能损伤。研究者通过脑室内注射氯磷酸脂质体后发现位于脑血管和脑膜的边缘相关巨噬细胞(BAMs)才是 IL-17 真正的“接头人”,从而参与了高血压患者的神经血管和认知功能损伤(Fig 4a-g)。
而神经皮质中的 ROS 产生酶 Nox2 是血管氧化应激的主要来源,在大脑皮层中应用 ROS 清除剂 MnTBAP 可挽救 DOCA 盐对功能性充血的损害(Fig 4h),证明 ROS 参与了神经血管功能障碍。随后利用 NovoCyte Quanteon 流式细胞仪检测了不同小鼠离体脑细胞的 ROS 表达,通过染色鉴定 BAMs(CD45hiCD11b+CD36+)、小胶质细胞 MG(CD45intCD11b+)和内皮细胞 EC(CD45-Ly6C+)三种细胞的 ROS 表达。结果发现 DOCA 增加了 BAMs 的 ROS 生成,但没有增加小胶质细胞或内皮细胞的 ROS 生成(Fig 4j)。
DOCA 不能增加 IL-17RA 缺陷小鼠 BAM 中的 ROS(Fig 4k),这表明 DOCA 高血压中 BAM ROS 的产生需要 IL-17 信号传导。为了进一步研究 IL-17RA 在 BAMs 中的作用,研究者利用骨髓嵌合小鼠模型,将 IL-17RA-/- 或 Nox2-/- BM 移植到 WT 小鼠体内,结果发现在 BAMs 中缺失 IL-17RA 或 Nox2 可完全防止功能性充血的损害(Fig 4n),并部分改善内皮血管活性(Fig 4o),同时嵌合小鼠表现出认知功能的改善,因此 IL-17RA 的激活才是诱发高血压脑部功能障碍的关键信号。
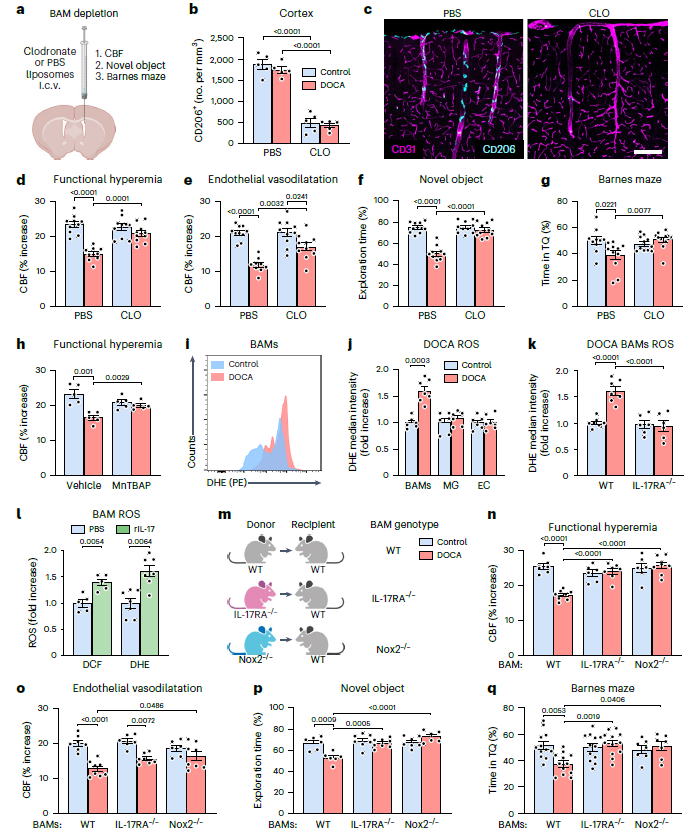
Fig4 . IL-17 在 BAMs 中通过 IL-17RA 介导的 ROS 生成增强作用损害功能性充血
03 硬脑膜 γδT17 细胞驱动高血压认知障碍
接下来,研究者为了提供证据支持硬脑膜中分泌 IL-17 的 T 细胞参与了 DOCA 盐高血压对神经血管和认知的影响。硬脑膜 γδT 细胞与其它 γδT 细胞一样是组织常驻细胞,在正常状态下,只有 1-2% 的细胞来自血液循环。然而,在炎症条件下,γδT 细胞涌入淋巴结并随后通过血液循环归巢到炎症组织。基于 DOCA 摄取后小鼠外周 TH17 和 γδT17 增多,因此研究者利用 SIPR 拮抗剂 FTY720 清除 TH17 和 γδT17 细胞,从而发现完全改善 DOCA 引起的神经充血和认知损伤。进一步利用 anti-TCRγδ antibody 发现硬脑膜分泌 IL-17 的 γδ T 细胞是导致盐敏感性高血压患者神经血管和认知功能受损的 IL-17 的来源。
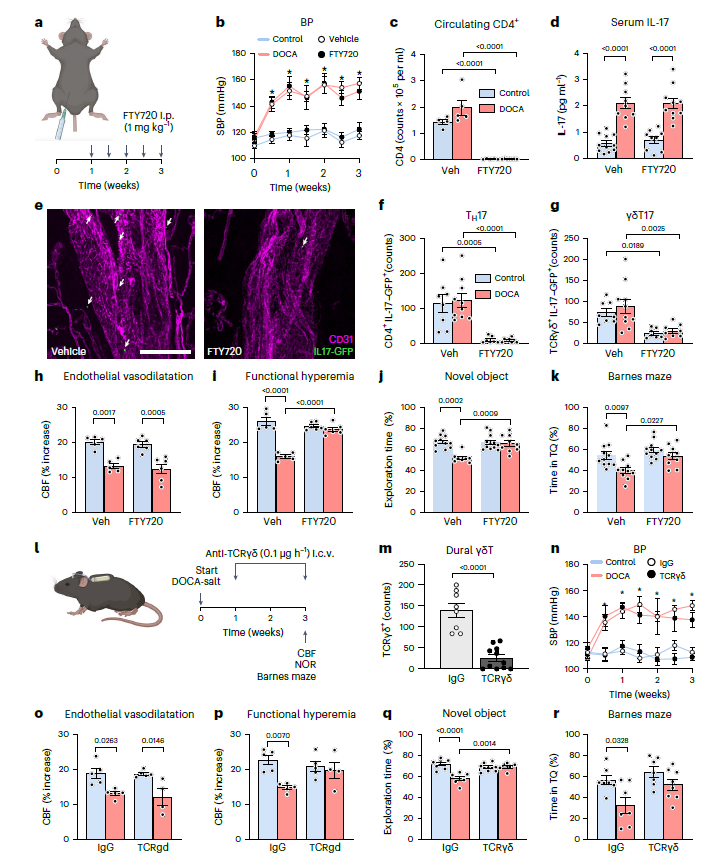
Fig 7. 盐敏感性高血压的认知障碍是由脑膜产生 IL-17 的 T 细胞驱动的
小结:本文揭示了盐敏感性高血压相关的神经血管损伤和认知功能障碍是由两种不同的机制介导的:
01 在血液循环中,T 细胞产生的 IL-17 作用于脑内皮 IL-17RA 以减少 NO 的产生,从而抑制内皮血管扩张,但不影响神经活动引起的 CBF 增加;
02 在大脑中,硬脑膜 T 细胞产生的 IL-17 作用于 BAMs 的 IL-17RA 以诱导血管氧化应激和抑制功能性充血,但对内皮功能的影响极小。
目前的降压治疗虽然能完全控制血压,但是不能完全缓解认知功能障碍。因此根据此研究,全面保护大脑可以针对脑膜进行免疫治疗,从而逆转大脑损伤。
此研究中,DOCA 盐诱导的高血压小鼠模型贯穿整个研究,因此对于原代小鼠细胞表型的鉴定也十分重要。威尔康奈尔医学院的 NovoCyte Quanteon 流式细胞仪是来自安捷伦科技公司的创新产品,其配备 4 激光器 25 个荧光通道,可满足绝大多数的免疫研究。高度自动化的配置让科研变得更简单有趣。同时采集与分析一体的自动化软件让科学家没有数据分析的后顾之忧。
BOOM!!!新品来袭!
2024 CYTO 会议上安捷伦发布了全新的 NovoCyte Opteon 全光谱流式细胞仪。可配置三到五个激光器,支持多达 73 个高性能检测通道,搭配双 SSC 检测,颗粒检测范围更宽,自发荧光扣除,为目标细胞群的鉴定提供更高的分辨率和灵敏度。它既满足了更多抗体染料组合的复杂流式配色方案,同时仍保留了 NovoCyte 系列产品简便易用的智能化特点。研究人员如今能以卓越的精度探索细胞的奥秘,并且可以同时分析多达 45 +个标志物,为流式细胞分析 panel 设计提供了极大的灵活性。
NovoCyte Opteon全光谱流式细胞仪






